菱镁矿的分解热力学和氢氧化镁的分解
- 发布人:管理员
- 发布时间:2014-05-15
- 浏览量:1366
【字体: 大 中 小 】
本篇专业知识主要内容是菱镁矿的分解热力学和氢氧化镁的分解,在耐火材料的生产和使用过程中,经常涉及热力学基础的应用,掌握菱镁矿的分解热力学有利于更好的了解镁质耐火材料生产的每个环节。
1菱镁矿的分解热力学
菱镁矿(MgCO3)的分解反应如下:
MgCO3(s)=MgO(s)+CO2 (g) (1)
MgCO3的分解压与温度的关系为:
lg(pCO2)=-6210/T+6.80 (2)
根据式(2)计算,在大气下MgCO3的化学沸腾温度为640.24℃。但实际的沸腾温度可能要要高一些。这是因为,MgCO3的分解速度较低,试样中的水不能完全去除,在分解时产生了副反应;以及含有杂质和形成固溶体等。
2 氢氧化镁的分解
氢氧化镁的分解反应为:
Mg(OH)2(s)=MgO(s)+H2O(g) (3)
与上述反应相关的热力学数据如表1所示。
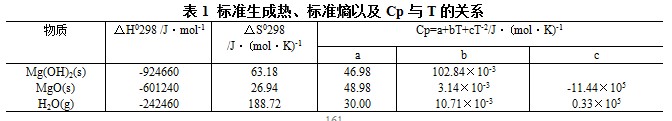
由上表可以求得Mg(OH)2分解反应的自由能随温度的变化关系如下:
△GΘT=80960-152.48T-32.0T(lnT/298+298/T-1)+44.5×10-3(T-298)2+6.24(T-298)2/T (4)
利用上式,并根据△GΘT=-RTln(pH2O),可以求出不同温度下由Mg(OH)2分解反应所产生的平衡分解压pH2O。
如果令pH2O=P=101.325kPa,那么可以由上述各关系式中求出Mg(OH)2的化学沸腾温度,为T=536K(263℃)。即,加热Mg(OH)2至263℃时,其分界压将与大气压相等。温度高于263℃,Mg(OH)2将发生剧烈分解,生成MgO。
下一篇:MgO-H2O体系热力学





